Revue Malgache de Biologie Clinique 2025; (1)1: 037-043
Etude de l’intérêt de l’acidification et de l’alcalinisation pour le dosage urinaire du calcium, magnésium, phosphate et acide urique sur automate BS300
Analysis of the acidification and alkalinization interest for the measurement of calcium, magnesium, phosphate and uric acid in the urine on a BS300 automaton.
SRV Rahajanirina1, F Totomandimby1, M Soja Rakotomalala1, A Rasamoelina2, L Andriamarohasina3, MK Ranaivosoa1
- Laboratoire de Biochimie, CHU JRA, Antananarivo, Madagascar
- Laboratoire d’hématologie, Antananarivo, Madagascar
- Institut Pasteur de Madagascar, Antananarivo, Madagascar
Auteur correspondant :
Rahajanirina Valdo
Email : ainavaldo@gmail.com
Adresse : Lot VT 85 Bis SA Andohanimandroseza
Téléphone : 0343840582
![]() Rmbc 2024007 (1.93 Mo)
Rmbc 2024007 (1.93 Mo)
Résumé
Introduction : pour des dosages urinaires fiables de calcium, magnésium, phosphate et acide urique, il est recommandé de requérir à un pré-traitement analytique des urines au laboratoire après le recueil urinaire. Plusieurs études menées sur différents types d’échantillons et automates ont préalablement démontré que ce traitement n’était pas nécessaire. L’objectif de cette étude est d’étudier la nécessité du traitement analytique sur des échantillons urinaires pour le dosage des 4 paramètres urinaires dosés sur l’analyseur Mindray BS300®.
Méthodes Il s’agit d’une étude prospective analytique menée au sein de l’unité paraclinique de recherche et de formation de Biochimie du Centre Hospitalier Universitaire Joseph Ravoahangy Andrianavalona. Une p value <0.05 a été considérée comme statistiquement significative. La méthode de régression de Passing Bablok et le coefficient de corrélation intra-classe ont été utilisés pour comparer les résultats sans et avec pré-traitement analytique des paramètres urinaires.
Résultats : Pour les 4 paramètres testés, aucune différence significative n’a été trouvée avec ou sans pré-traitement analytique. Une forte relation linéaire positive entre les variables comparées a été observée. Le coefficient de corrélation intra-classe a été supérieur à 0,9 indiquant un excellent accord entre les variables comparées.
Conclusion : Les résultats présentés montrent que l’acidification/alcalinisation d’échantillons urinaires n’est pas une nécessité analytique pour les dosages de calcium, phosphore, magnésium et acide urique sur BS300®.
Mots clés : acidification, alcalinisation, traitement analytique, urines.
Abstract
Introduction : For reliable measurements of calcium, phosphate, magnesium and uric acid in the urine, it is recommended to collect urine and require its pre- analytical treatment in laboratory. Many studies conducted analysis on different types of samples and automaton have previously proved that this treatment is not required. The purpose of this analysis is to study the need for urine samples analytical process in order to have the measurement of 4 urinary parameters as per the dosage from the Mindray BS300® analyzer.
Methods : It’s a prospective analytical study, conducted within the paraclinical research and training unit of Biochemistry at the Joseph Ravoahangy Andrianavalona University Hospital. A p value <0.05 was considered as statistically significant. The Passing Bablok regression method and the intraclass correlation coefficient were used to compare the results without and with pre- analytical treatment of urinary parameters.
Results : From the 4 tested parameters, there was no significant differences with or without pre- analytical treatment. A strong positive linear relationship between the compared variables was noticed. The intraclass correlation coefficient was higher than 0.9, which indicated an excellent agreement between the compared variables.
Conclusion: The presented results demonstrated that the urine samples acidification/alkalinization is not an analytical requirement for the measurements of calcium, phosphate, magnesium and uric acid on BS300.
Keywords: acidification, alkalinization, analytical treatment, urine.
- INTRODUCTION
Les paramètres urinaires tels que le calcium, le magnésium, le phosphate et l'acide urique sont déterminés dans le cadre de l'enquête de laboratoire de routine chez les patients souffrant d'urolithiase en raison de l'importance de ces paramètres dans la formation des calculs [1,2]. Il est recommandé qu’une acidification préalable de l’échantillon urinaire par une solution acide à faible volume pour le dosage du calcium, du magnésium, et du phosphate dans les urines. Et pour le dosage de l’acide urique urinaire, l’addition de base permet de dissoudre les solutés précipités [2,3]. Plusieurs études menées sur différents types d’échantillons et automates ont préalablement démontré que ce traitement n’était pas nécessaire. [4-7]
Les manipulations de l’acide chlorhydrique (HCl) et de la soude (NaOH) 5% ont des effets néfastes pour la santé des manipulateurs à cause du risque chimique mais aussi pour les automates car les sondes et les tubulures peuvent être endommagées par ces pH extrêmes. A notre connaissance, aucune étude sur la détermination de la nécessité de l’acidification ou de l’alcalinisation des paramètres biochimiques urinaires n’ a été menée sur l’automate Mindray BS300®.
L’ajout d’acide ou de base dans les échantillons urinaires à doser ne modifierait pas les résultats de ces paramètres à tester. L’objectif de cette étude est d’étudier la nécessité du traitement analytique sur des échantillons urinaires pour le dosage du calcium, du phosphate, du magnésium et de l’acide urique urinaire dosés sur l’analyseur Mindray BS300®.
Il s’agit d’une étude prospective analytique menée à l’unité paraclinique de formation et de recherche (UPFR) de Biochimie du Centre Hospitalier Universitaire Joseph Ravoahangy Andrianavalona (CHU-JRA) sur une période de 4 mois allant du 30 mai 2022 au 31 septembre2022.Toutes les urines de 24 heures conformes aux conditions pré-analytiques parvenues dans le service ont été incluses dans cette étude.
L’acidification pour le dosage du calcium, du magnésium et du phosphate a été réalisée par ajout de 70 μL d’HCl pour 5mL d’urine, pour cibler un pH inférieur à 2 comme recommandé par le fournisseur et par les études précédentes, notamment pour assurer la dissolution des cristaux d’oxalate de calcium [2]. Après homogénéisation, le pH a été vérifié par bandelettes réactives (Linear Cromatest®) et papier pH, et si nécessaire ajusté pour obtenir le pH ciblé. L’alcalinisation des échantillons urinaires pour le dosage de l’acide urique a été réalisée par ajout de 50 μl de NaOH 5 % pour 5 ml d’urine, pour cibler un pH supérieur à 8. De même, après homogénéisation, le pH a été vérifié par bandelettes réactives, et si nécessaire ajusté pour obtenir le pH ciblé. Les échantillons urinaires ont été préalablement centrifugés, puis dosés selon le circuit habituel du laboratoire sur BS300® (Mindray). Les méthodes de dosage des analytes étudiées sont les suivantes : méthode colorimétrique en point final utilisant la complexation avec l’arsenazo III pour le calcium urinaire, méthode photométrique à 340 nm utilisant la complexation avec le molybdate d’ammonium pour le phosphate urinaire, méthode colorimétrique en point final pour le magnésium urinaire et une méthode photométrique en point final après réaction de Trinder avec le couple uricase-peroxydase pour l’acide urique urinaire.
La saisie des textes et des tableaux a été faite sur le logiciel Word XP®. Pour tous les résultats, la moyenne et l’écart type ont été calculés. Une p value <0.05 a été considérée comme statistiquement significative. Les résultats des paramètres urinaires avec et sans acidification ont été comparés selon la méthode de régression de Passing Bablok et le coefficient de corrélation intra-classe.
Le diagramme de Bland et Altman a été aussi utilisé. Le graphique de Bland-Altman est un diagramme de dispersion dans lequel la différence entre les mesures appariés A-B est représentée par rapport à leur valeur moyenne.
- Résultats
Au total, 33 échantillons ont été inclus dans l'étude.
- Comparaison entre les résultats de dosage urinaire du calcium, du magnésium, du phosphate et d’acide urique sans et avec prétraitement
Aucune différence significative des paramètres étudiés n’a été détectée entre les échantillons non traités et traités par l’acidification ou alcalinisation (Tableau I et II).
Tableau I. Comparaison entre les résultats de dosage urinaire du calcium, du magnésium, du phosphate et de l’acide urique sans et avec pré-traitement (acidification/alcalinisation)
|
Analytes (urinaire) N=33 (mmol/l) |
Moyenne ± ET ou médiane (min, max) |
Moyenne ± ET ou médiane (min, max) |
p value p<0.05 |
|
Non acidifié |
Acidifié |
|
|
|
Calcium |
0,06±1,32
6,01±1,32 |
0,08±1,46
5,80±1,46 |
NS |
|
Magnésium |
0,05±1,20
4,60±1,20 |
0,10±1,33
5,01±1,33
|
NS |
|
Phosphate |
2,65±4,31
25,26±4,31 |
2,75±4,67
25,43±4,67 |
NS |
|
|
Non alcalinisé |
Alcalinisé |
|
|
Acide urique
|
0,58±1,93 8,05±1,93 |
0,42±1,90 8,25±1,90 |
NS |
.
*NS : Non significatif
- Résultats de la corrélation entre les dosages du calcium, du magnésium, du phosphate et de l’acide urique dans les échantillons urinaires avant et après traitement
- Calciurie
La corrélation entre calciurie sans acidification (x) et avec acidification (y) fournit une équation de régression y = -0,0557 + 1,011 avec une droite de pente 1,011 et d'origine 0,00557 avec un coefficient de corrélation r = 0,970 (intervalle de confiance à 95 %, IC = 0,970) ce qui correspond à un très bon accord entre les deux variables. Ainsi, il n’y a pas de différence entre les deux variables.
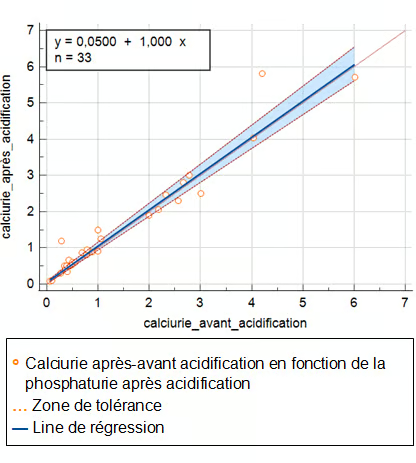
Figure 1 : Corrélation entre les concentrations de la calciurie dans les échantillons avec et sans acidification
Une représentation graphique de Bland et Altman pour étudier la concordance des deux variables a été également réalisée. Une forte relation linéaire positive entre les deux variables a été trouvée. Le coefficient de corrélation intra-classe (CCIC= 0.968) supérieur à 0,9 indique un excellent accord entre les deux variables.
La figure 2 a montré la relation brute entre concentration de phosphate avant acidification en abscisse et après acidification en ordonnée. La relation est de type linéaire (r =0,99), avec une pente de 1,104 et une ordonnée à l’origine de -0,5931. La régression linéaire de la concentration en phosphate avant et après acidification a montré une très bonne corrélation (r = 0,99). Aucune différence ou déviation significative n’a été observée.
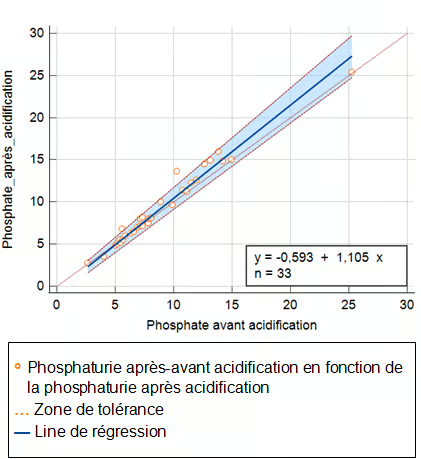
Figure 2 : Corrélation entre les concentrations de phosphate urinaire dans les échantillons avec et sans acidification
Selon le diagramme différence de Bland et Altman, le coefficient de corrélation entre les deux méthodes est r = 0,99 (IC à 95% [0,938 - 0,990]) et le coefficient de corrélation intra-classe de la Phosphaturie (CCIC) égale à 0.978 (supérieur à 0,9) indiquant un excellent accord entre les deux variables. Une corrélation positive entre le phosphate urinaire avant et après acidification a été observée.
2.3 Magnésurie
Le diagramme de Passing et Bablok (figure 3) indique la ligne de régression entre les deux méthodes ; et l'équation de régression est y = -0,0465 + 1.112, pour la pente de 1.011. La corrélation entre magnésium urinaire (mmol) sans prétraitement (x) et avec acidification(y) fournit une droite de pente 1.112 et d'origine 0.0465 avec un coefficient de corrélation r = 0,97 (intervalle de confiance à 95 %, IC = 0,970).
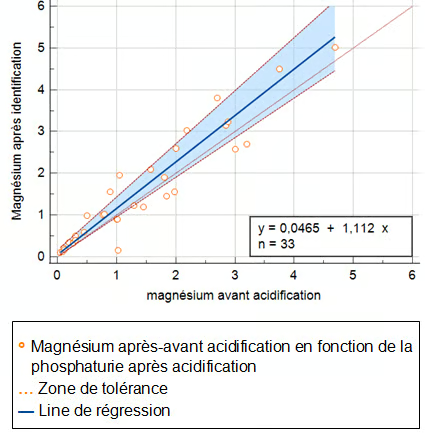
Figure 3: Corrélation entre les concentrations de magnésium urinaire dans les échantillons avec et sans acidification
Le coefficient de corrélation entre les deux valeurs de magnésurie avant et après acidification est r = 0,95 (IC à 95% [0,871 - 0,969]) et le coefficient de corrélation intra-classe de la magnésurie (CCIC) égale à 0,93 (supérieur à 0,9) indiquant un excellent accord entre les deux variables. Une corrélation positive entre le phosphate urinaire avant et après acidification a été constatée.
2.4 Uricurie
D’après le diagramme de passing et Bablok (figure 4), il existe une très bonne corrélation entre la concentration d’acide urique avant et après alcalinisation (r = 0,999).
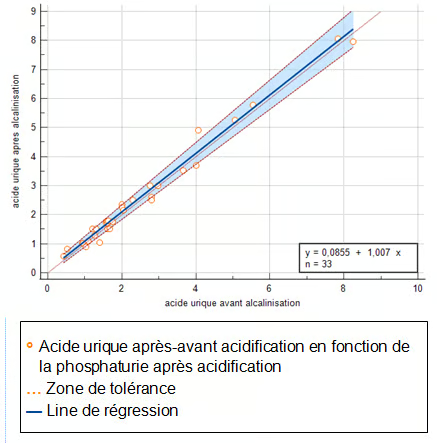
Figure 4 : Corrélation entre les concentrations de l’acide urique urinaire dans les échantillons avec et sans alcalinisation
D’après le diagramme de différence de Bland et Altman, le coefficient de corrélation entre les deux méthodes est r = 0,99 (IC à 95% [0,982 - 0,996]) et le coefficient de corrélation intra-classe de l’acide urique (CCIC) égale à 0.991 (supérieur à 0,9) indiquant un excellent accord entre les deux variables. Une corrélation positive entre l’acide urique urinaire avant et après acidification (r=0.99) a été observée.
L’analyse urinaire joue un rôle clé dans le diagnostic différentiel ou étiologique de nombreuses maladies rénales et urologiques.
Le pH joue un rôle très important dans la solubilité de nombreux composants des cristaux urinaires. Les propriétés de solubilité du calcium, de l'acide urique sont assez différentes. Lorsque l’urine est alcaline, le phosphate a tendance à se précipiter facilement. En revanche lorsque l’urine est acide (pH <5,5), c’est l’acide urique qui se cristallise. Comme la cristallisation, la précipitation conduit également à la formation d’une phase solide cristallisée ; dans ce cas précis, par réaction chimique. La précipitation apparait lorsque certains anions comme OH-, Cl- s’unissent avec des cations métalliques (Ca2+, Ag+, etc.) et forme ainsi des composés insolubles. Ainsi, pour un pH à 8,0, le calcium qui précipite dans l'urine alcaline sous forme de phosphate de calcium, a perdu à un taux initial de 12 % par minute, contre 5 % pour l'oxalate [5]. De ce fait, il faudrait prendre en compte que ce phénomène peut conduire à une sous-estimation du résultat du dosage urinaire de ce paramètre.
En plus, compte tenu des risques pour la sécurité du personnel de laboratoire, l’addition d’un acide ou d’une base aux échantillons urinaires au niveau du laboratoire représente de nombreux inconvénients : risque pour le technicien, dilution des échantillons, consommation de temps et nécessité d’un espace de prétraitement des échantillons.
- Calcium, magnésium et phosphate urinaires
Pour le dosage du calcium, du phosphate et du magnésium dans les urines, nos résultats n’ont montré aucune différence significative avec ou sans pré-traitements des échantillons et il existe une très bonne corrélation entre la concentration de ces paramètres biochimiques avant et après acidification de l'urine.
Ces résultats correspondaient à ceux de l’étude de Yilmaz et al. menée dans un laboratoire de biochimie clinique en Turquie en 2008 qui n’a pas non plus trouvé de différence significative entre les résultats de dosage de ces paramètres sans ou avec acidification [6].
Nos résultats concordaient également avec ceux des autres études menées dans d’autres laboratoires, à condition que les échantillons soient analysés rapidement après réception [4,6-11].
Contrairement à une étude menée par Pratumvinit et al. en 2013 qui a montré que les concentrations de calcium et de phosphate ont été significativement différentes dans tous les échantillons, avec ou sans cristaux ; tandis que les concentrations de magnésium ont été significativement différentes uniquement dans les échantillons avec cristaux [12].
Une étude faite par Mostaghat et al. en 2019, aucune différence significative n’a été observée chez les patients lithiasiques [13].
Nos résultats ont montré une discordance avec ceux de l’étude menée par Ng RH et al. qui ont trouvé une différence significative entre l’échantillon pré-traité et non [14].
L’acide urique est formé d’un noyau pyrimidique et d’un noyau imidazolé. Selon les conditions du milieu, l’acide urique peut être sous deux formes : la forme moléculaire ou la forme ionisée plus communément appelée urate. L’acide urique est un composé chimique de formule brute C5H4N4O3. C’est un acide faible de pKa 5,7. Selon le pH du milieu dans lequel se trouve l’acide urique, l’équilibre sera déplacé vers la formation de la forme moléculaire pour un pH<pKa ou vers la forme ionisée pour un pH>pKa. Comme le premier proton de l’acide urique a un pKa de 5,47, la majeure partie de l’acide urique se trouve sous forme non dissociée quand le pH urinaire est inférieur à 5,5 [15].
Au pH physiologique (7,35-7,45), l'acide urique est à 98% sous forme ionisée.
Il est présent à 37°C dans le plasma sous forme d'urate de sodium à une concentration d’environ 420 µmol/L. L'acide urique et l'urate sont des molécules relativement insolubles qui précipitent facilement dans des solutions aqueuses telles que l'urine ou le liquide synovial, pouvant provoquer des lithiases ou des arthrites.Il constitue le produit final du métabolisme des bases puriques qui peut être d’origine endogène ou exogène [16].
Selon les recommandations, il a été suggéré que pour le dosage de l’acide urique urinaire, l’addition d’une base permet de dissoudre les solutés précipités. Avec un pH à 6,5, presque 100 % de l'acide urique est sous forme d'urate soluble. Plus le pH augmente, plus la solubilité de l'acide urique est grande. Le pH de l'urine stérile est habituellement acide et permet à l'acide urique d'exister sous forme non dissociée. La sursaturation urinaire en acide urique non dissocié est dictée par trois facteurs: le pH, la concentration en cations et la concentration d'acide urique.
C’est pour cela que notre étude a pour but de vérifier la recommandation du fournisseur à propos du pré-traitement par alcalinisation pour le dosage de l’acide urique urinaire. D’après nos résultats, aucune différence significative entre les valeurs de l’acide urique urinaire sans et avec alcalinisation n’a été observée.
Une étude de Petit M et al. en 2017 a révélé une très bonne corrélation entre la concentration d’acide urique avant et après alcalinisation, et aucun déviant n’a été observé. Aucune différence significative n’a été mise en évidence après alcalinisation lorsque l’uricurie est inférieure au seuil de 2,5 mmol/L [11].
Une étude de Larcher L et al. en 2017 a montré que l’absence d’ajustement du pH urinaire en vue du dosage du calcium et de l’acide urique entraîne une sous-estimation du bilan urinaire pouvant induire une erreur diagnostique chez des patients lithiasiques dont la cristallurie est positive pour des cristaux calcium-dépendants ou d’acide urique [17].
Cette étude est limitée par le petit nombre d’échantillons. Une étude plus étendue et approfondie chez les patients lithiasiques devrait être menée. Elle ne permet pas de savoir si l'acidification ou l'alcalinisation a un impact sur la conservation des échantillons car les dosages ont été effectués très rapidement juste après prélèvement. Une étude de stabilité des échantillons est souhaitable.
Conclusion
Les analyses des paramètres urinaires ne sont pas négligeables. Elles doivent être réalisées dans de bonnes conditions. Un des rôles des biologistes est d’assurer la fiabilité et la qualité des résultats rendus.
Cette étude vise à déterminer la nécessité du pré-traitement analytique de quelques paramètres biochimiques urinaires tels que la calciurie, la phosphaturie, la magnésurie et l’uricurie.
D’après nos résultats, aucune différence significative n’a été trouvée sans ou avec pré-traitement pour tous les paramètres testés et il existe une forte relation linéaire positive entre les variables comparées. Les coefficients de corrélation intra-classe ont été tous supérieurs à 0.9 indiquant un excellent accord entre les variables comparées.
Ainsi, l’acidification ou l’alcalinisation d’échantillons urinaires pour le dosage de ces paramètres n’était pas nécessaire.
Remerciements
Nous adressons nos sincères remerciements au Directeur d’Etablissement du CHUJRA pour nous avoir autorisé la réalisation de ce présent travail. De même, nos remerciements vont à l’endroit de tout le personnel de l’UPFR Biochimie du CHUJRA notamment les techniciens de laboratoire qui ont permis la bonne conduite de la présente étude en respectant les normes exigées.
Conflit d'intérêt : aucun
REFERENCES
- Daudon M, Traxer O, Jungers P. Lithiase urinaire. Médecine-Sciences-Flammarion, Paris; 2012.
- Daudon M, RéveillaudRJ.Typage morphologique des calculs oxalocalciques et données étiopathogéniques. Sem Hôp Paris. 1986,62:3159-68.
- Hodgkinson A. Sampling errors in the determination of urine calcium and oxalate: solubility of calcium oxalate in HCl-urine mixtures. ClinChimActa. 1981;109: 239-44.
- Sodi R, Bailey LB, Glaysher J, Allars L et al. Acidification and urine calcium: is it a preanalytical necessity? Ann ClinBiochem. 2009; 46: 484-7.
- Sodi R, Godber IM. Effect of refrigeration, centrifugation, acidification,heat treatment and storage on urine calcium, magnesium and phosphate. ClinChem Lab Med. 2016;54 : e379-e81.
- Yilmaz G, Yilmaz FM, Hakligör A, Yücel D. Are preservatives necessary in 24-hour urine measurements? ClinBiochem. 2008; 41: 899-901.
- Feres MC, Bini R, De Martino MC, Biagini SP et al. Implications for the use of acid preservatives in 24-hour urine for measurements of high demand biochemical analytes inclinical laboratories. ClinChimActa. 2011; 412:2322-5.
- Wu W, Yang D, Tiselius HG, Ou L et al. Collection and storage of urine specimens for measurement of urolithiasis risk factors. Urology. 2015; 85: 299-303.
- Simkin PA, Hoover PL, Paxson CS, Wilson WF. Uric acid excretion: quantitative assessment from spot, midmorning serum and urine samples. Ann Intern Med.1979; 91. 44-47.
- McConnell W, Vasikaran SD. Spot urine analysis: acidification does not increase calcium recovery. Ann ClinBiochem 2002; 39: 64- 65.
- Petit M, Beaudeux JL, Majoux S, Hennequin C. De la nécessité d’un traitement pré-analytique des urines pour les dosages de calcium, phosphate et acide urique ? Ann Biol Clin. 2017; 75(5):519‑24.
- Pratumvinit B, Reesukumal K, Wongkrajang P, Khejonnit V et al. Should acidification of urine be performed before the analysis of calcium, phosphate and magnesium in the presence of crystals? Clin Chim Acta.2013;426:46-50.
- MostaghatI, Bailleul S, Lefèvre G., Frochot V.Relations entre aspect urinaire, cristaux et acidification dans le dosage du calcium chez les patients lithiasiques. JibInnov.2019; 423: 46-51.
- Ng RH, Menon M, Ladenson JH. Collection and handling of 24-hoururine specimens for measurement of analytes related to renal calculi. ClinChem1984; 30: 467-71.
- Coe Fl, Parks JH. Uric acid stones. In: Nephrolithiasis: pathogenesis and treatment. 2nd edition.Year Book Medical Publishers, Chicago 1988: 250-68.
- Holmes EW. Uric acid nephrolithiasis. In : Coe FL, Brenner BM, Stein JH, eds Contemporary issues in nephrology : nephrolithiasis. New York: Churchill-Livingstone, 1980, 188-207.
- Larcher L, Lefevre G, Bailleul S, Daudon M, et al. Importance of pre-analytical for urinalysis with urinary crystals. Ann Biol Clin. 2017; 75:525-30.
